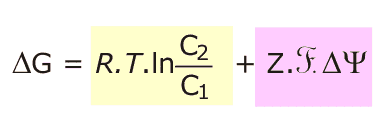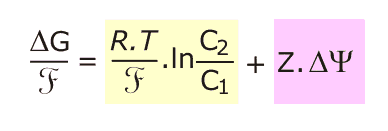2 Teoría Básica
![]()
2.1
VARIACIÓN DE ENERGÍA LIBRE EN EL TRANSPORTE
La magnitud termodinámica de interés en los procesos de
transporte de un soluto a través de una membrana es el denominado Potencial
Electroquímico del soluto. Se define como la variación de energía libre que
ocurre cuando se transporta un mol del soluto a través de una membrana
manteniendo constantes tanto las concentraciones del soluto en los compartimentos de llegada y
de salida como el potencial de membrana. Es pues una magnitud que tiene sentido asumiendo condiciones
de estado estacionario durante el proceso de transporte.
El potencial electroquímico viene dado por la expresión:
|
|
Siendo: R la constante de los gases (8,314 J/º.mol); T, la temperatura absoluta F, la constante de Faraday (96.480 J/mol.V). C1 y C2 son las concentraciones de soluto libre en los compartimentos de salida y llegada, respectivamente. Z es la carga del soluto, con el signo adecuado. DY: diferencia de potencial en voltios entre ambos compartimentos (Potencial del de llegada menos potencial de salida) |
Si DG es negativo, el transporte es exergónico, y no requiere aporte de energía externa para llevarse a cabo; si DG es positivo, el transporte es endergónico, y requiere un aporte externo de energía. Es decir, se requiere un proceso exergónico que suministre la energía necesaria y un mecanismo de acoplamiento que transfiera la energía desde el proceso exergónico al transporte endergónico.
Es importante tener en cuenta lo siguiente:
1
C1 y C2 son concentraciones de
soluto libre (más correctamente
habría que hablar de actividades del soluto). Y no tienen que coincidir
necesariamente con las concentraciones de soluto totales, ya que puede ocurrir
que el soluto esté unido a otras moléculas en uno o en ambos compartimentos; en ese caso la concentración
del soluto TOTAL puede ser mucho mayor que la del soluto libre. Por ejemplo, el
oxígeno en el eritrocito no se encuentra libre, sino unido en su mayor parte a
la hemoglobina; la concentración de oxígeno libre es muy pequeña, pero la
cantidad de oxígeno total es elevada.
2
Obviamente, en el caso de que el
soluto no esté cargado, el segundo término de la ecuación se anula.
3
Es importante tener en cuenta que
los dos términos de la expresión son independientes, y es perfectamente posible
que el primer término, correspondiente a las concentraciones, sea positivo, y
el segundo negativo, o viceversa. Lo importante, lo que va a definir si el
transporte es exergónico o endergónico, es la suma de ambos.
4
El potencial electroquímico, tal
como se ha definido, presupone que tanto las concentraciones como el potencial
de membrana son constantes durante el proceso de transporte.
Es un estado estacionario. Esta condición es,
evidentemente, una simplificación. De hecho, cuando se trata de solutos
cargados, el potencial de membrana cambia rápidamente con el movimiento de los
iones de uno a otro lado de la membrana, de tal forma que en muy poco tiempo
las condiciones pueden ser radicalmente diferentes de las que existían al
principio del proceso.
Según la expresión #1, el potencial electroquímico se expresa en Julios.mol-1. Si se dividen ambos términos de la expresión por la constante de Faraday, se puede expresar el potencial electroquímico en voltios:
En el caso de que el soluto transportado sea el H+ , la ecuación anterior se puede expresar de la siguiente forma:
DpH es el pH del compartimento de llegada menos el pH del compartimento de salida (note el signo menos en el término de concentración). DmH+ es el potencial electroquímico del protón o fuerza protonmotriz (pmf, protonmotive force), por analogía a la fuerza electromotriz. Con este nombre, Peter Mitchell (Premio Nobel en 1978) quiso resaltar la capacidad de producir trabajo de estos gradientes de iones hidronio, hidrogeniones (o menos correctamente, protones).
|
tabla: fuerza protonmotriz en varios sistemas |
![]()
CLASIFICACIÓN DE LOS PROCESOS DE TRANSPORTE
El primer criterio que se aplica a la hora de
clasificar los procesos de transporte es el termodinámico: ¿El transporte es exergónico
o endergónico?. En el caso de que el transporte sea exergónico, es decir, el
soluto se mueva A FAVOR de su potencial electroquímico, se trata de TRANSPORTE
PASIVO. Si, por el contrario, el soluto se transporta EN CONTRA de su potencial
electroquímico (transporte endergónico), se trata de TRANSPORTE ACTIVO.
El segundo criterio se refiere al mecanismo
concreto que permite al soluto atravesar la bicapa lipídica. Hay que recordar que en la inmensa
mayoría de los casos los solutos son moléculas polares o iónicas, y para ellas
la zona hidrofóbica de la bicapa lipídica supone una barrera insalvable: la
permeabilidad de las bicapas lipídicas para las moléculas polares del tamaño de
la glucosa o mayores, y para los iones, es prácticamente nula. Por consiguiente, tiene
que haber un mecanismo que permita a estas moléculas e iones atravesar la bicapa lipídica. Como es de esperar, son diferentes tipos de proteínas las que
llevan a cabo esta tarea. Tenemos los siguientes casos:
el número se refiere a la clasificación presente
en el esquema
Transporte independiente de proteínas
0 Difusión simple o libre. El soluto es suficientemente soluble en la membrana como para atravesarla sin problemas. Es importante exclusivamente en el caso del oxígeno, o del nitrógeno para los organismos diazotrofos. De hecho, ambos gases son más solubles en medio hidrofóbico que en medio acuoso.
Se pensaba que el agua era una molécula suficientemente pequeña para poder atravesar la bicapa lipídica, “infiltrándose” entre las cadenas desordenadas de los ácidos grasos. Sin embargo, el descubrimiento de que prácticamente todos los organismos presentan unas proteínas que permiten el paso del agua a través de las membranas, las denominadas acuaporinas, hace pensar que la difusión simple del agua carece de importancia real.
Transporte dependiente de proteínas.
Difusión
facilitada. El soluto se mueve a
favor de su potencial electroquímico a través de la membrana, pero la atraviesa
gracias a la existencia de una proteína que facilita esa difusión. Hay dos posibilidades:
1 La proteína se limita a crear un conducto hidrofílico por el que el soluto se mueve libremente. Son los Poros y Canales.
|
|
|
2 La proteína une al soluto, y lo mueve a través de la membrana gracias a un cambio conformacional. La proteína es un transportador (carrier) en sentido estricto. Dado que en el caso de la difusión facilitada sólo se transporta un tipo de soluto, recibe la denominación especial de Uniporte.
|
|
|
Tanto la difusión simple como la difusión
facilitada son procesos de Transporte
Pasivo, ya que en ambos casos el transporte es exergónico. El Transporte Activo requiere siempre de
la existencia de una proteína. Hay varias posibilidades:
2 Transporte activo secundario. (Cotransporte)
El
transporte de un soluto en contra de su potencial electroquímico puede ser
acoplado por un transportador adecuado al transporte exergónico de otro soluto. El primero se transporta activamente,
aprovechando la energía liberada por el
transporte pasivo del segundo a favor de su potencial electroquímico. El mecanismo es análogo al del uniporte
3 Transporte Activo Primario. (Bombas)
El transporte se acopla a una reacción química exergónica (por ejemplo, hidrólisis de ATP) o a la luz, que suministran la energía necesaria para transportar al soluto en contra de su potencial electroquímico. A este tipo especial de transportadores se les denomina “Bombas”.

4 Traslocación de grupo.
El soluto
es transportado y modificado covalentemente de un modo simultáneo
 |
 |